La leucemia linfática aguda (LLA) y el sarcoma de Ewing, con incidencia en la población infantil, son posibles candidatos para desarrollar estrategias terapéuticas basadas en CRISPR, según las investigaciones de la Unidad de Citogenética Molecular y Edición Génica del Centro Nacional de Investigaciones Oncológicas (CNIO).
Así lo ha explicado a EFEsalud el investigador del CNIO y del Instituto Josep Carreras Raúl Torres-Ruiz tras participar en un ponencia sobre CRISPR en oncología en el transcurso del IV Foro “La Oncología Médica en 3 días” que hoy se clausura en el Teatro Goya de Madrid.
“Con el tiempo, todos los tumores van acumulando distintas mutaciones genéticas, pero algunos tipos, como la leucemia mieloide crónica, son adictos a la expresión de un solo evento, la translocación de dos cromosomas que genera un nuevo gen de fusión con características oncogénicas”, similar a una mutación en un gen, indica.
También es el caso del sarcoma de Ewing, un cáncer oseo que afecta a adolescentes y niños, y en el que se abre una vía de tratamiento, o el caso de la leucemia mieloide crónica que se debe a la traslocación cromosómica en los genes BCR y ABL.

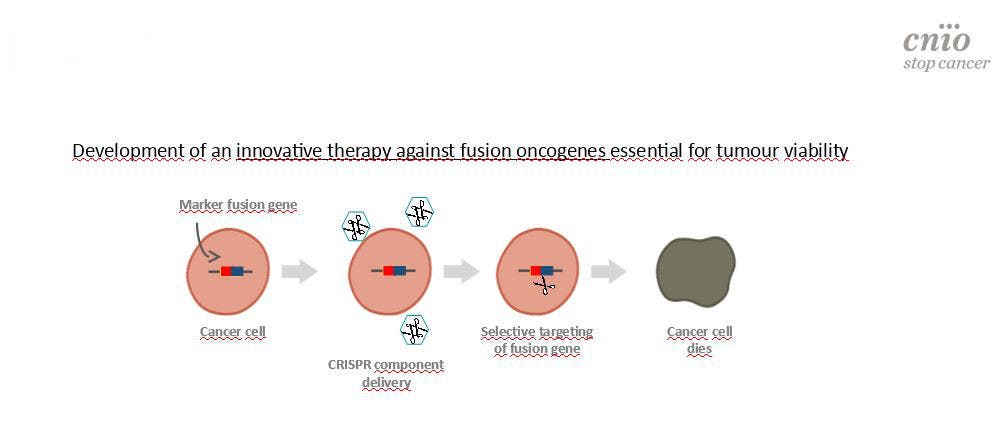
“Si conseguimos impactar sobre esos genes de fusión seríamos capaces de atacar la base de ese cáncer, pero eso solo ocurriría en un 20% de los cánceres y en una parte de ese porcentaje es donde, por ahora, hemos visto que se puede aplicar el CRISPR”, apunta el científico.
Pero no se trataría de corregir o sustituir en el tumor esa translocación cromosómica, como sí se hace en los casos de mutaciones en genes que provocan otras enfermedades.
“En el cáncer no corregiríamos la mutación, la atacaríamos de forma que solo llegaría a las células tumorales y se eliminarían”, manifiesta Torres-Ruiz quien resalta que el objetivo es introducir un vector que llegue a todas las células malignas posibles y de forma específica para que provoque la muerte celular.
Y esa actuación se haría cuando el tumor ya está diagnosticado ya que se trata de mutaciones que no se han heredado, sino que aparecen de novo y a partir de ahí se desarrolla el cáncer.
Esta técnica se podría plantear en un futuro como una estrategia terapéutica coadyuvante, en combinación con otros tratamientos como, por ejemplo, la extirpación del tumor.
Otra de las aplicaciones en cáncer es la modificación de los linfocitos T “para que se hagan resistentes a la inactivación por parte del tumor” y puedan combatirlo.
Se trata de las terapias CAR T (Chimeric Antigen Receptor T-Cells), una de las técnicas más avanzadas de transferencia celular adoptiva que está mostrando efectividad en leucemia linfoblástica aguda, en niños y mayores, y en linfoma y mieloma múltiple en adultos.
También la Unidad de Citogenética Molecular y Edición Génica del CNIO, dirigida por la doctora Sandra Rodríguez-Perales, investiga la aplicación de CRISPR en glioma (tumor cerebal) o neuroblastoma (en el tejido nervioso) pero, en general, se trata de tumores específicos ya que si algo caracteriza al cáncer es su gran complejidad derivada de la variedad de mutaciones genéticas.
CRISPR en enfermedades monogénicas
En el lado opuesto del cáncer se encuentran las enfermedad monogénicas o causadas por un solo gen en donde la terapia génica a través de CRISPR puede tener un gran potencial.
Son los casos de la anemia de Fanconi o la distrofia muscular de Duchenne donde ya se ha utilizado la terapia génica en la práctica clínica.
“Por eso nos planteamos tratar unos tipos de cáncer que son parecidos, que no igual, a las enfermedades monogénicas al predominar una mutación principal”, señala el científico del CNIO.
Pero la edición genética en cáncer todavía se circunscribe en la investigación básica, al laboratorio con células y modelos animales. Todavía queda camino por recorrer.




Debe estar conectado para enviar un comentario.