Las CAR T (Chimeric Antigen Receptor T-Cells) son una de las técnicas más avanzadas de transferencia celular adoptiva y está mostrando efectividad en leucemia linfoblástica aguda, en niños y mayores, y en linfoma y mieloma múltiple en adultos.
Los resultados de los ensayos clínicos muestran que, en leucemia linfoblástica aguda, un 80-90% de los pacientes responde al tratamiento, pero al año recae un 30-35%, por lo que la tasa de supervivencia libre de enfermedad se sitúa en un 50% a los doce meses.
“Es un éxito tremendo para casos desesperados que ya habían probado otras líneas de tratamiento sin resultado, como el trasplante alogénico de médula ósea. Todavía no hay datos sólidos a dos años del tratamiento pero hay altas expectativas de que se mantenga esa respuesta”, explica a EFEsalud el director del Instituto de Hematología y Oncología del Hospital Clinic de Barcelona, el doctor Álvaro Urbano-Ispizua.
El 80% de los niños con leucemia linfoblástica aguda, un tipo de cáncer de la sangre minoritario (afecta a 1-2 personas por cada 100.000 habitantes/año), consigue superar la enfermedad con los tratamientos de quimioterapia convencionales, pero el otro 20% no responde. Es precisamente este menor porcentaje de niños el que se está beneficiando de las terapias CAR T, además de otros pacientes adultos con la misma enfermedad.
La tasa de respuesta en el caso del linfoma es del 40%, inferior al de la leucemia (80%), pero sin embargo el número de recaídas es mínimo, por lo que la tasa de supervivencia libre de progresión al cabo de un año en linfoma se mantiene casi en ese 40%.
“En el caso del linfoma sí podemos decir, al cabo de dos años, que más de una tercera parte de los pacientes se mantienen sin enfermedad y es muy posible que curados porque un linfoma si no da la cara en dos años es que ya no existe”, señala el hematólogo, también coordinador del Grupo Español CAR, de investigación y práctica clínica, de la Sociedad Española de Hematología y Hemoterapia (SEHH)
Todavía se desconoce por qué unos pacientes responden a la terapia CAR T y otros no, como ocurre con otros tratamientos de inmunoterapia en otros tipos de cáncer hematológico y sólido.
Pero lo que sí se sabe es la razón por la que se producen recaídas tras esta terapia celular que, en el caso de la leucemia linfoblástica aguda, afecta a un 30-35% de los pacientes tratados al cabo de un año, tanto pediátricos como adultos.
“La razón es porque algunas células leucémicas pierden la diana y con una sola célula sin diana a la que atacar, el CAR no va a ser eficaz, no la va a detectar. Y si nadie la ataca se hace fuerte, se expande y vuelve la enfermedad”, manifiesta el especialista.
“Otra causa de recaída -añade- es que el propio CAR T también puede quedar exhausto y al cabo de dos o tres meses la enfermedad reaparace”.
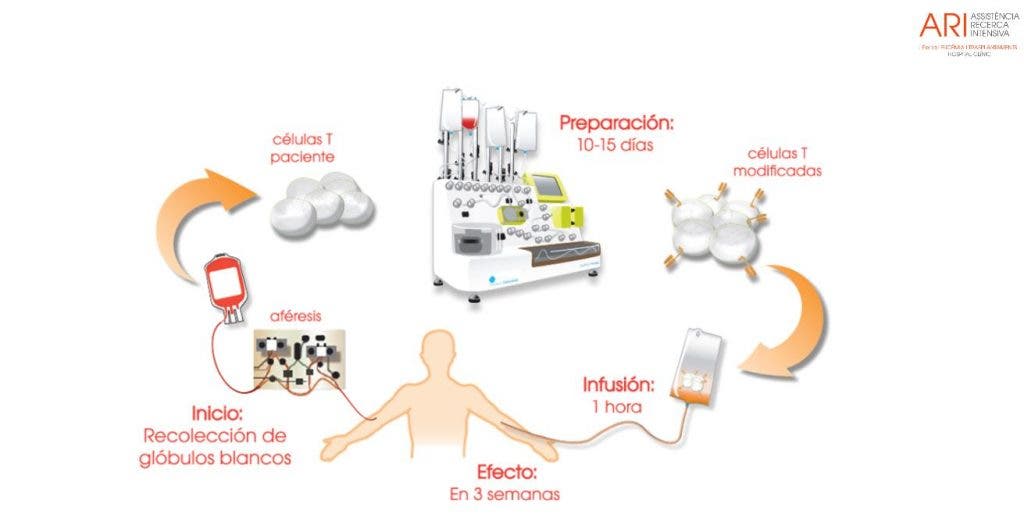
¿Cómo funciona un CAR T?
El sistema inmunológico no es lo suficientemente eficaz para eliminar por sí mismo todas las células tumorales. Por eso es necesario estimularlo. Es el tratamiento de inmunoterapia.
El proceso comienza con una toma de sangre del paciente con cáncer hematológico de donde se extraen los linfocitos T, células del sistema inmunológico, que estaban activos contra las células cancerígenas pero que no eran capaces de destruirlas.
Esos linfocitos son tratados para introducirles dos genes elaborados en laboratorio que le proporcionan, por una parte, potencia y proliferación y, por otra, lo dirigen como un rayo láser contra la célula cancerosa y no contra el resto de tejidos, explica el investigador. Esta es otra de las estrategias punteras contra la enfermedad, la terapia génica.

El gen 1 tiene el fin de convertir al linfocito en un láser que se dirige directo a la diana de la célula cancerígena, una proteína que se expresa a modo de receptor. Ese gen, un anticuerpo monoclonal, se dirige de forma precisa a la célula tumoral y no al resto. Una tercera terapia, la terapia dirigida.
El gen 2 corresponde a una molécula coestimulatoria. Se encuentra en el propio linfocito de forma natural, pero al volver a introducirlo en esa célula inmunitaria se coloca pegado al gen 1, y así produce una especie de cortocircuito y comienza una proliferación que antes se frenaba de forma natural, ya que de lo contrario nuestro sistema inmune serían tan potente que nos provocaría enfermedades autoinmunes sin control.
Y es ese segundo botón, el gen 2, el que se inserta en el linfocito y cuando este, a la primera señal del gen 1, toca la célula cancerosa se activa directamente.
El doctor Urbano-Ispizua explica: “Nuestro sistema inmunológico tiene un freno y es que para actuar necesita una especie de segunda señal. La primera señal es detectar la diana contra la que actuar, pero el segundo botón nuclear tiene que estar activado también para que esa célula ejerza el efecto destructor sobre la diana”.
Para que esos genes lleguen a los linfocitos se utiliza un virus como vehículo que los infecta de forma natural. Una vez dentro de los linfocitos, estos se cultivan con factores de crecimiento y el resultado es que se multiplica por 40 la cantidad de linfocitos extraídos del paciente.
“Cuando se reinfunden al paciente esos linfocitos multiplicados y detectan las células cancerígenas son capaces de multiplicarse de nuevo cada uno de ellos por diez, por cien, por mil…hasta conseguir destruir la enfermedad”, señala el doctor.
Los linfocitos T modificados genéticamente, los CAR T, se convierten así en “supersoldados” que han proliferado formando un ejército que se dirige de forma precisa contra las células tumorales.
Los efectos secundarios
El tratamiento consiste, por lo general, en una sola transfusión al paciente con los linfocitos modificados que pervive durante meses o años. Pero algunos enfermos desarrollan efectos secundarios.
El principal es consecuencia de la proliferación de linfocitos que produce unas sustancias tóxicas para el paciente, un proceso llamado síndrome de liberación de citocinas.
“Hasta un 30% de los pacientes tratados con CAR T tienen que ser internados en una Unidad de Cuidados Intensivos (UCI) por problemas con el oxígeno, presión arterial, coagulación sanguínea… pero por suerte existe una especie de antídoto, un bloqueante de las citocinas, que hace que el paciente responda satisfactoriamente”, señala el doctor Álvaro Urbano-Ispizua
La segunda complicación que puede aparecer, en menor número de casos, es una toxicidad en el sistema nervioso. “Pero se resuelve espontáneamente y no necesita tratamiento”, puntualiza.
“Después de superar estas complicaciones, estamos observando que no quedan secuelas y repercute en la calidad de vida del paciente”, subraya.
Proyecto Ari de terapia CAR T
El doctor Álvaro Urbano-Ispizua conoce bien los datos de los ensayos clínicos realizados en Estados Unidos y en Europa donde las agencias del medicamento ya han dado luz verde a algunos fármacos de CAR T.
Pero el hematólogo también lo ha comprobado directamente como director del Proyecto Ari que lidera el Hospital Clínic de Barcelona, al diseñar un medicamento CAR T académico, es decir, con donaciones de particulares y pendiente de recibir financiación pública del Instituto de Salud Carlos III en cuanto prueben eficacia y seguridad y reciban la autorización de la Agencia Española del Medicamento.
Este desarrollo está en proceso de terminar la fase I del ensayo clínico con 39 pacientes y en junio de 2019 tiene previsto iniciar la fase II con 30 pacientes. Con estas dos fases se considera probado el medicamento, como ocurre con los CAR financiados por la industria.
“Los pacientes son adultos y niños con leucemia linfoblástica aguda y linfoma repartidos entre once hospitales españoles. En el Hospital Clínic fabricamos los medicamentos CAR T y los distribuiremos a los hospitales con estos pacientes”, apunta el especialista.
La vuelta a la normalidad de los pacientes
Uno de esos hospitales es el Sant Joan de Deu, en Espugles de Llobregat (Barcelona), que ha colaborado con pacientes pediátricos desde la fase I del CAR Ari, además de ser el primer centro en España que participó, en enero de 2016, en un ensayo clínico internacional con el CAR T desarrollado por la compañía farmacéutica Novartis indicado para niños y jóvenes menores de 25 años en fase avanzada de leucemia linfoblástica aguda.

La doctora Susana Rives, responsable de la Unidad de Leucemias y Linfomas del Servicio de Hematología y Oncología del citado hospital, ha vivido en primera fila la experiencia obtenida con las terapias CAR T en niños y jóvenes ya sin otras alternativas de tratamiento.
Aunque algunos desarrollan las toxicidades antes mencionadas y otros, muy pocos, no responden al tratamiento, “son terapias que consiguen respuestas largas y quizá curación, aunque todavía es pronto para decirlo, pero puede cambiar la historia natural de la enfermedad”, asegura la hematóloga pediátrica.
En los casos de respuesta, “me asombra la calidad de vida que tienen después del tratamiento con CAR T. Las familias nos preguntan por qué no se lo hemos dado antes. Hay niños que vuelven al colegio al cabo de un mes, llevan una vida normal, con energía”.
Como tratamiento en sí es menos agresivo que la quimioterapia y el trasplante alogénico. Una vez al mes necesitan volver al hospital a recibir anticuerpos, defensas que refuercen su organismo.
Pero se trata de leucemias y linfomas en los que son los linfocitos B los que se malignizan y a los que atacan las terapias CAR T, los linfocitos T modificados, no otros subtipos de cánceres de la sangre.
El hospital Sant Joan de Deu tiene previsto participar en los próximos meses en otro ensayo clínico, simultáneo en Estados Unidos y Europa, para comprobar la efectividad del CAR de Novartis en pacientes con fases menos avanzadas de leucemia linfoblástica aguda para administrar ese tratamiento tras la quimioterapia y en lugar del trasplante alogénico de médula ósea.
CAR T académicos y CAR T comerciales
Nueve grupos de investigación en España trabajan actualmente en el desarrollo de fármacos CAR T académicos (sin financiación de la industria farmacéutica) que, además de leucemias y linfomas, van dirigidos también contra el mieloma múltiple.
Tres compañías farmacéuticas han apostado por la terapia CAR T. Novartis y Gilead tienen fármacos aprobados ya por la Agencia Europea del Medicamento y están pendientes de la luz verde de las autoridades sanitarias españolas, mientras que el de Celgene tiene en trámite su aprobación en Europa.
¿Medicamentos complementarios o competidores? Todavía es algo que está en el aire como también lo están los precios de unos y otros.
Unos tratamientos innovadores que en Estados Unidos tienen un coste de entre 350.000 y 450.000 dólares por paciente, mientras que el coste de un CAR T académico se calcula que ronda los 80.000-100.000 euros por enfermo.
El presidente de la Sociedad Española de Hematología y Hemoterapia (SEHH), Jorge Sierra, ha pedido a la administración que impulse la investigación en terapias CAR T en el ámbito académico y ha dado el respaldo al Plan del Ministerio de Sanidad para asegurar un acceso equitativo y seguro a estas terapias en el Sistema Nacional de Salud.
“Pedimos, respecto a los CAR T comerciales, un plan de acceso rápido y que el precio sea lo más ajustado posible”, concluye el presidente de la sociedad médica.





Debe estar conectado para enviar un comentario.